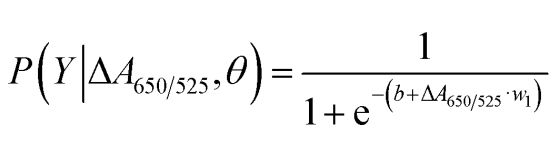La detecció precoç del càncer basada en la biòpsia líquida és una nova direcció de detecció i diagnòstic del càncer proposada pel National Cancer Institute dels EUA en els darrers anys, amb l'objectiu de detectar càncer precoç o fins i tot lesions precanceroses. S'ha utilitzat àmpliament com a nou biomarcador per al diagnòstic precoç de diverses malalties malignes, com ara el càncer de pulmó, els tumors gastrointestinals, els gliomes i els tumors ginecològics.
L'aparició de plataformes per identificar biomarcadors del paisatge de metilació (Methylscape) té el potencial de millorar significativament el cribratge precoç del càncer, situant els pacients en la fase més primerenca tractable.
Recentment, els investigadors han desenvolupat una plataforma de detecció senzilla i directa per a la detecció del paisatge de metilació basada en nanopartícules d'or decorades amb cisteamina (Cyst/AuNPs) combinades amb un biosensor basat en telèfons intel·ligents que permet una detecció precoç ràpida d'una àmplia gamma de tumors. La detecció precoç de la leucèmia es pot realitzar en 15 minuts després de l'extracció d'ADN d'una mostra de sang, amb una precisió del 90,0%. El títol de l'article és Detecció ràpida d'ADN cancerós en sang humana mitjançant AuNPs cobertes amb cisteamina i un telèfon intel·ligent habilitat per a l'aprenentatge automàtic.
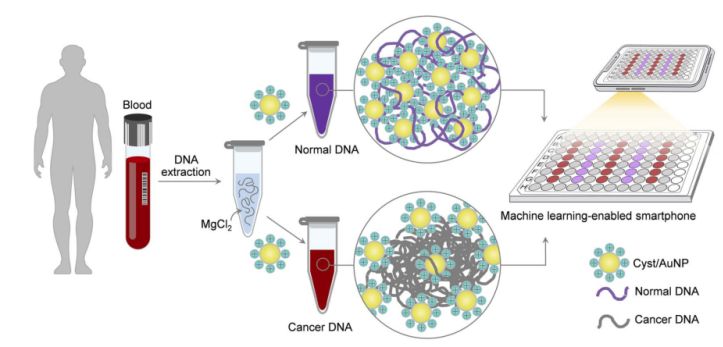
Figura 1. Una plataforma de detecció senzilla i ràpida per al cribratge del càncer mitjançant components de quist/AuNPs es pot aconseguir en dos senzills passos.
Això es mostra a la Figura 1. Primer, es va utilitzar una solució aquosa per dissoldre els fragments d'ADN. A continuació, es van afegir Cyst/AuNPs a la solució barrejada. L'ADN normal i el maligne tenen propietats de metilació diferents, la qual cosa resulta en fragments d'ADN amb patrons d'autoacoblament diferents. L'ADN normal s'agrega de manera laxa i finalment agrega Cyst/AuNPs, la qual cosa provoca el desplaçament cap al vermell de les Cyst/AuNPs, de manera que es pot observar un canvi de color de vermell a porpra a simple vista. En canvi, el perfil de metilació únic de l'ADN cancerós condueix a la producció de grups més grans de fragments d'ADN.
Es van prendre imatges de plaques de 96 pous amb la càmera d'un telèfon intel·ligent. L'ADN del càncer es va mesurar amb un telèfon intel·ligent equipat amb aprenentatge automàtic en comparació amb mètodes basats en espectroscòpia.
Cribratge del càncer en mostres de sang reals
Per ampliar la utilitat de la plataforma de detecció, els investigadors van aplicar un sensor que distingia amb èxit entre ADN normal i cancerós en mostres de sang reals. Els patrons de metilació als llocs CpG regulen epigenèticament l'expressió gènica. En gairebé tots els tipus de càncer, s'ha observat que els canvis en la metilació de l'ADN i, per tant, en l'expressió dels gens que promouen la tumorigènesi s'alternen.
Com a model per a altres càncers associats amb la metilació de l'ADN, els investigadors van utilitzar mostres de sang de pacients amb leucèmia i controls sans per investigar l'eficàcia del paisatge de metilació en la diferenciació dels càncers leucèmics. Aquest biomarcador del paisatge de metilació no només supera els mètodes de cribratge ràpid de leucèmia existents, sinó que també demostra la viabilitat d'estendre'l a la detecció precoç d'una àmplia gamma de càncers mitjançant aquest assaig senzill i directe.
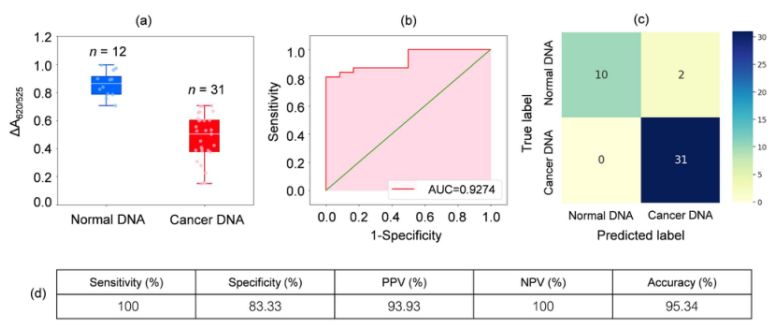
Es va analitzar l'ADN de mostres de sang de 31 pacients amb leucèmia i 12 individus sans. Com es mostra al diagrama de caixa de la Figura 2a, l'absorbància relativa de les mostres de càncer (ΔA650/525) era inferior a la de l'ADN de mostres normals. Això es va deure principalment a la hidrofobicitat augmentada, que va provocar una densa agregació d'ADN de càncer, cosa que va impedir l'agregació de Cyst/AuNPs. Com a resultat, aquestes nanopartícules es van dispersar completament a les capes externes dels agregats de càncer, cosa que va provocar una dispersió diferent de Cyst/AuNPs adsorbits en agregats d'ADN normal i de càncer. A continuació, es van generar corbes ROC variant el llindar des d'un valor mínim de ΔA650/525 fins a un valor màxim.
Figura 2.(a) Valors d'absorbància relativa de solucions de quist/AuNPs que mostren la presència d'ADN normal (blau) i cancerós (vermell) en condicions optimitzades.
(DA650/525) de diagrames de caixa; (b) Anàlisi ROC i avaluació de proves diagnòstiques. (c) Matriu de confusió per al diagnòstic de pacients normals i amb càncer. (d) Sensibilitat, especificitat, valor predictiu positiu (VPP), valor predictiu negatiu (VPN) i precisió del mètode desenvolupat.
Com es mostra a la Figura 2b, l'àrea sota la corba ROC (AUC = 0,9274) obtinguda per al sensor desenvolupat va mostrar una alta sensibilitat i especificitat. Com es pot veure al diagrama de caixa, el punt més baix que representa el grup d'ADN normal no està ben separat del punt més alt que representa el grup d'ADN del càncer; per tant, es va utilitzar la regressió logística per diferenciar entre els grups normal i el càncer. Donat un conjunt de variables independents, estima la probabilitat que es produeixi un esdeveniment, com ara un grup de càncer o normal. La variable dependent oscil·la entre 0 i 1. Per tant, el resultat és una probabilitat. Vam determinar la probabilitat d'identificació del càncer (P) basant-nos en ΔA650/525 de la següent manera.
on b=5.3533,w1=-6.965. Per a la classificació de mostres, una probabilitat inferior a 0,5 indica una mostra normal, mentre que una probabilitat de 0,5 o superior indica una mostra de càncer. La figura 2c representa la matriu de confusió generada a partir de la validació creuada de "leave-it-alone", que es va utilitzar per validar l'estabilitat del mètode de classificació. La figura 2d resumeix l'avaluació de la prova diagnòstica del mètode, incloent-hi la sensibilitat, l'especificitat, el valor predictiu positiu (VPP) i el valor predictiu negatiu (VPN).
Biosensors basats en telèfons intel·ligents
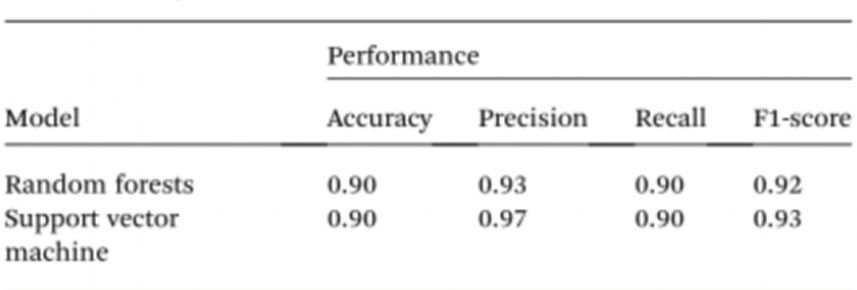
Per simplificar encara més les proves de mostres sense l'ús d'espectrofotòmetres, els investigadors van utilitzar la intel·ligència artificial (IA) per interpretar el color de la solució i distingir entre individus normals i cancerosos. Tenint en compte això, es va utilitzar la visió per computador per traduir el color de la solució de Cyst/AuNPs a ADN normal (morat) o ADN cancerós (vermell) utilitzant imatges de plaques de 96 pous preses a través de la càmera d'un telèfon mòbil. La intel·ligència artificial pot reduir costos i millorar l'accessibilitat en la interpretació del color de les solucions de nanopartícules, i sense l'ús de cap accessori de maquinari òptic per a telèfons intel·ligents. Finalment, es van entrenar dos models d'aprenentatge automàtic, incloent Random Forest (RF) i Support Vector Machine (SVM), per construir els models. Tant el model RF com el SVM van classificar correctament les mostres com a positives i negatives amb una precisió del 90,0%. Això suggereix que l'ús de la intel·ligència artificial en la biosensorització basada en telèfons mòbils és força possible.
Figura 3. (a) Classe diana de la solució enregistrada durant la preparació de la mostra per al pas d'adquisició d'imatges. (b) Exemple d'imatge presa durant el pas d'adquisició d'imatges. (c) Intensitat del color de la solució de quist/AuNPs a cada pou de la placa de 96 pous extreta de la imatge (b).
Utilitzant Cyst/AuNPs, els investigadors han desenvolupat amb èxit una plataforma de detecció senzilla per a la detecció del paisatge de metilació i un sensor capaç de distingir l'ADN normal de l'ADN cancerós quan s'utilitzen mostres de sang reals per al cribratge de leucèmia. El sensor desenvolupat va demostrar que l'ADN extret de mostres de sang reals era capaç de detectar de manera ràpida i rendible petites quantitats d'ADN cancerós (3 nM) en pacients amb leucèmia en 15 minuts, i va mostrar una precisió del 95,3%. Per simplificar encara més les proves de mostres eliminant la necessitat d'un espectrofotòmetre, es va utilitzar l'aprenentatge automàtic per interpretar el color de la solució i diferenciar entre individus normals i cancerosos mitjançant una fotografia de telèfon mòbil, i també es va poder aconseguir una precisió del 90,0%.
Referència: DOI: 10.1039/d2ra05725e
Data de publicació: 18 de febrer de 2023
 中文网站
中文网站