Nat Med | Un enfocament multiòmic per cartografiar el paisatge tumoral, immunitari i microbià integrat del càncer colorectal revela la interacció del microbioma amb el sistema immunitari
Tot i que els biomarcadors del càncer de còlon primari s'han estudiat àmpliament en els darrers anys, les directrius clíniques actuals només es basen en l'estadificació tumor-gangli limfàtic-metàstasi i la detecció de defectes de reparació de desajustos d'ADN (MMR) o inestabilitat de microsatèl·lits (MSI) (a més de les proves de patologia estàndard) per determinar recomanacions de tractament. Els investigadors han observat una manca d'associació entre les respostes immunitàries basades en l'expressió gènica, els perfils microbians i l'estroma tumoral a la cohort de càncer colorectal de l'Atles del Genoma del Càncer (TCGA) i la supervivència dels pacients.
A mesura que ha progressat la recerca, s'ha informat que les característiques quantitatives del càncer colorectal primari, inclosa la naturalesa cel·lular, immunitària, estromal o microbiana del càncer, es correlacionen significativament amb els resultats clínics, però encara hi ha una comprensió limitada de com les seves interaccions afecten els resultats dels pacients.
Per disseccionar la relació entre la complexitat fenotípica i el resultat, un equip d'investigadors de l'Institut Sidra d'Investigació Mèdica de Qatar ha desenvolupat i validat recentment una puntuació integrada (mICRoScore) que identifica un grup de pacients amb bones taxes de supervivència combinant les característiques del microbioma i les constants de rebuig immunitari (ICR). L'equip ha realitzat una anàlisi genòmica exhaustiva de mostres fresques congelades de 348 pacients amb càncer colorectal primari, incloent-hi la seqüenciació d'ARN de tumors i teixit colorectal sa coincident, la seqüenciació de l'exoma complet, la seqüenciació del gen del receptor de cèl·lules T profundes i del rRNA bacterià 16S, complementada amb la seqüenciació del genoma tumoral complet per caracteritzar encara més el microbioma. L'estudi es va publicar a Nature Medicine com a "Un atles integrat de tumors, immunitari i microbioma del càncer de còlon".

Article publicat a Nature Medicine
Informació general de l'AC-ICAM
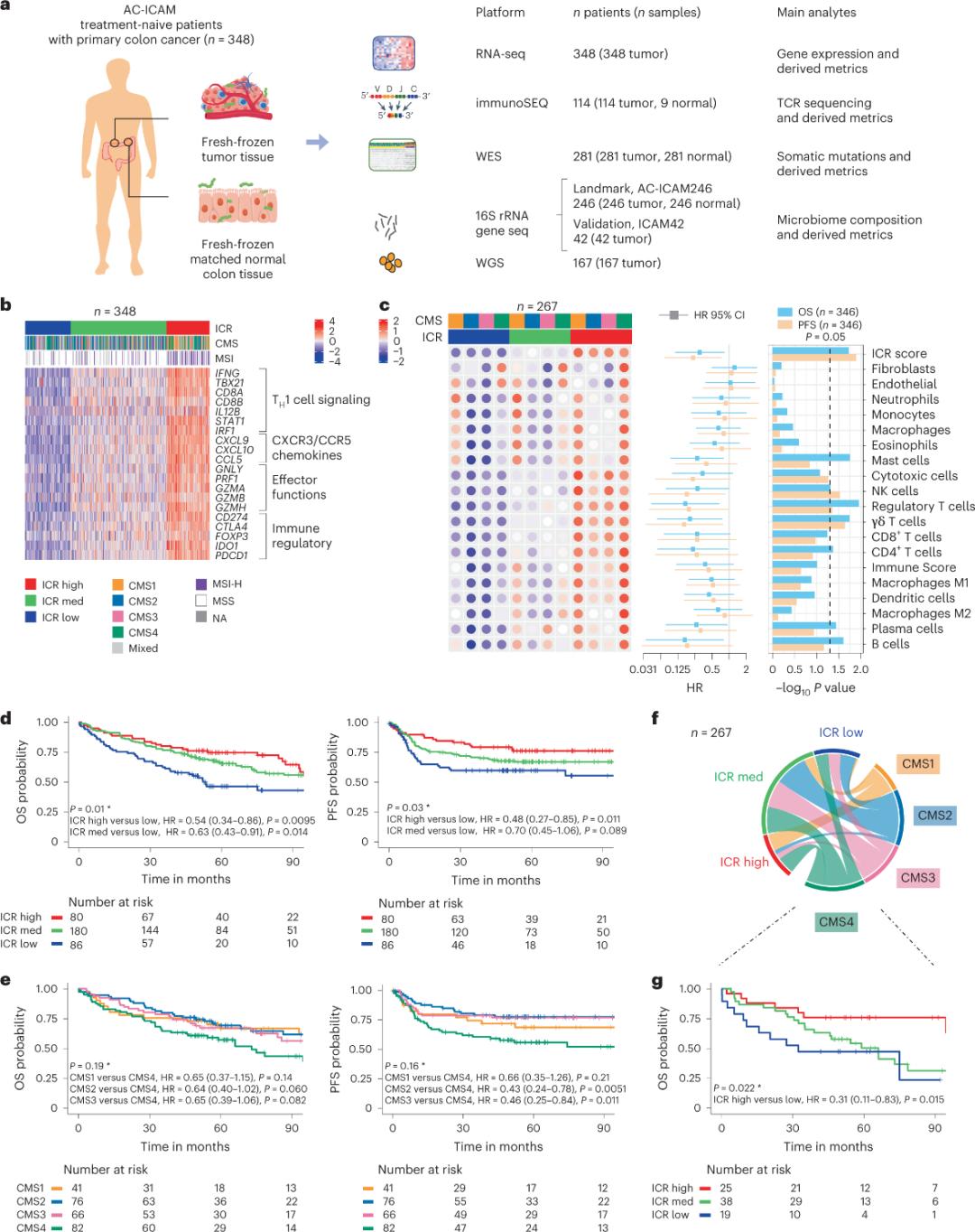
Els investigadors van utilitzar una plataforma genòmica ortogonal per analitzar mostres tumorals fresques congelades i van emparellar teixit de còlon sa adjacent (parells tumor-normal) de pacients amb un diagnòstic histològic de càncer de còlon sense teràpia sistèmica. Basant-se en la seqüenciació de l'exoma complet (WES), el control de qualitat de les dades de RNA-seq i la detecció dels criteris d'inclusió, es van retenir dades genòmiques de 348 pacients i es van utilitzar per a anàlisis posteriors amb un seguiment mitjà de 4,6 anys. L'equip de recerca va anomenar aquest recurs Sidra-LUMC AC-ICAM: Un mapa i una guia de les interaccions immune-cancer-microbiome (Figura 1).
Classificació molecular mitjançant ICR
L'equip de recerca, capturant un conjunt modular de marcadors genètics immunitaris per a la immunovigilància contínua del càncer, anomenat constant immunitària de rebuig (ICR), va optimitzar l'ICR condensant-lo en un panell de 20 gens que cobreix diferents tipus de càncer, com ara el melanoma, el càncer de bufeta i el càncer de mama. L'ICR també s'ha associat amb la resposta a la immunoteràpia en diversos tipus de càncer, inclòs el càncer de mama.
Primer, els investigadors van validar la signatura ICR de la cohort AC-ICAM, utilitzant un enfocament de coclassificació basat en gens ICR per classificar la cohort en tres clústers/subtipus immunitaris: ICR alta (tumors calents), ICR mitjana i ICR baixa (tumors freds) (Figura 1b). Els investigadors van caracteritzar la propensió immunitària associada amb subtipus moleculars de consens (CMS), una classificació del càncer de còlon basada en el transcriptoma. Les categories CMS incloïen CMS1/immunitari, CMS2/canònic, CMS3/metabòlic i CMS4/mesenquimal. L'anàlisi va mostrar que les puntuacions ICR estaven correlacionades negativament amb certes vies de cèl·lules canceroses en tots els subtipus CMS, i només es van observar correlacions positives amb vies immunosupressores i relacionades amb l'estroma en els tumors CMS4.
En tots els CMS, l'abundància de subconjunts de cèl·lules assassines naturals (NK) i cèl·lules T va ser més alta en els subtipus d'immunitat alta amb ICR, amb una major variabilitat en altres subconjunts de leucòcits (Figura 1c). Els subtipus immunitaris amb ICR van tenir diferents OS i PFS, amb un augment progressiu de l'ICR de baixa a alta (Figura 1d), validant el paper pronòstic de l'ICR en el càncer colorectal.
Figura 1. Disseny de l'estudi AC-ICAM, signatura gènica relacionada amb la immunitat, subtipus immunitaris i moleculars i supervivència.
L'ICR captura cèl·lules T enriquides amb tumors i amplificades clonalment
Només s'ha informat que una minoria de cèl·lules T que s'infiltren en el teixit tumoral són específiques per a antígens tumorals (menys del 10%). Per tant, la majoria de les cèl·lules T intratumorals es denominen cèl·lules T espectadores (cèl·lules T espectadores). La correlació més forta amb el nombre de cèl·lules T convencionals amb TCR productius es va observar en subpoblacions de cèl·lules estromals i leucòcits (detectats per RNA-seq), que es poden utilitzar per estimar les subpoblacions de cèl·lules T (Figura 2a). En els clústers ICR (classificació general i CMS), la clonalitat més alta dels TCR SEQ immunitaris es va observar en els grups ICR-alt i CMS subtipus CMS1/immunitaris (Figura 2c), amb la proporció més alta de tumors ICR-alt. Utilitzant tot el transcriptoma (18.270 gens), sis gens ICR (IFNG, STAT1, IRF1, CCL5, GZMA i CXCL10) es trobaven entre els deu primers gens positivament associats amb la clonalitat de SEQ immunitari TCR (Figura 2d). La clonalitat del TCR d'ImmunoSEQ es va correlacionar més fortament amb la majoria dels gens ICR que les correlacions observades utilitzant marcadors CD8+ sensibles al tumor (Figura 2f i 2g). En conclusió, l'anàlisi anterior suggereix que la signatura ICR captura la presència de cèl·lules T enriquides amb tumors i amplificades clonalment, i pot explicar les seves implicacions pronòstiques.
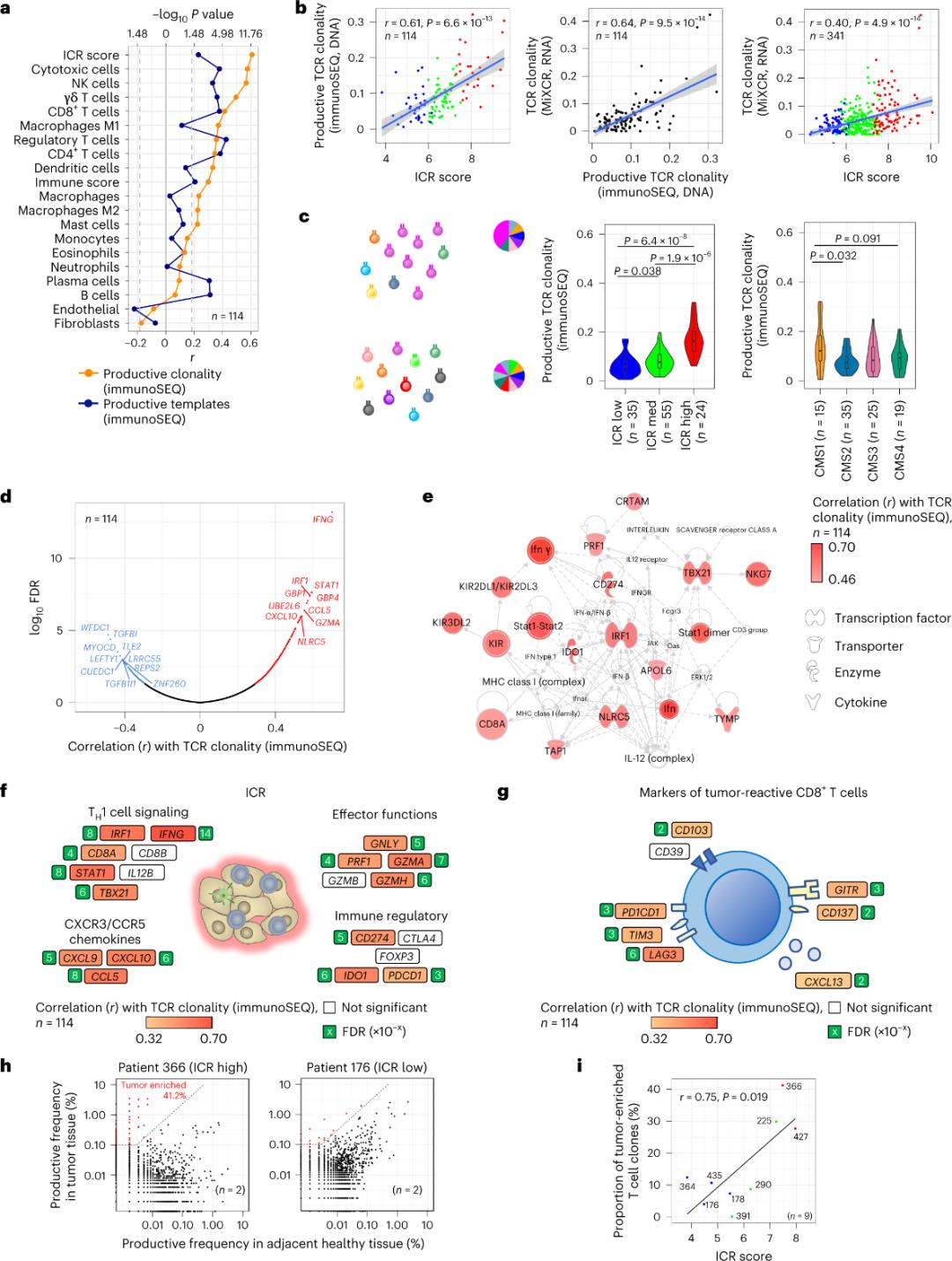
Figura 2. Mètriques de TCR i correlació amb gens relacionats amb la immunitat, subtipus immunitaris i moleculars.
Composició del microbioma en teixits sans i de càncer de còlon
Els investigadors van realitzar la seqüenciació de l'ARNr 16S utilitzant ADN extret de teixit tumoral i de còlon sa coincident de 246 pacients (Figura 3a). Per a la validació, els investigadors van analitzar addicionalment les dades de seqüenciació del gen ARNr 16S de 42 mostres tumorals addicionals que no tenien ADN normal coincident disponible per a l'anàlisi. Primer, els investigadors van comparar l'abundància relativa de flora entre els tumors coincidents i el teixit colon sa. El Clostridium perfringens va augmentar significativament en els tumors en comparació amb les mostres sanes (Figura 3a-3d). No hi va haver cap diferència significativa en la diversitat alfa (diversitat i abundància d'espècies en una sola mostra) entre les mostres tumorals i les sanes, i es va observar una reducció modesta de la diversitat microbiana en els tumors amb ICR alt en relació amb els tumors amb ICR baix.
Per detectar associacions clínicament rellevants entre els perfils microbians i els resultats clínics, els investigadors van intentar utilitzar dades de seqüenciació del gen rRNA 16S per identificar les característiques del microbioma que prediuen la supervivència. A AC-ICAM246, els investigadors van executar un model de regressió OS Cox que va seleccionar 41 característiques amb coeficients diferents de zero (associats amb el risc de mortalitat diferencial), anomenades classificadors MBR (Figura 3f).
En aquesta cohort d'entrenament (ICAM246), una puntuació MBR baixa (MBR < 0, MBR baixa) es va associar amb un risc de mort significativament menor (85%). Els investigadors van confirmar l'associació entre una MBR baixa (risc) i una OS prolongada en dues cohorts validades independentment (ICAM42 i TCGA-COAD). (Figura 3) L'estudi va mostrar una forta correlació entre els cocos endogàstrics i les puntuacions MBR, que eren similars en el teixit tumoral i el teixit colònic sa.
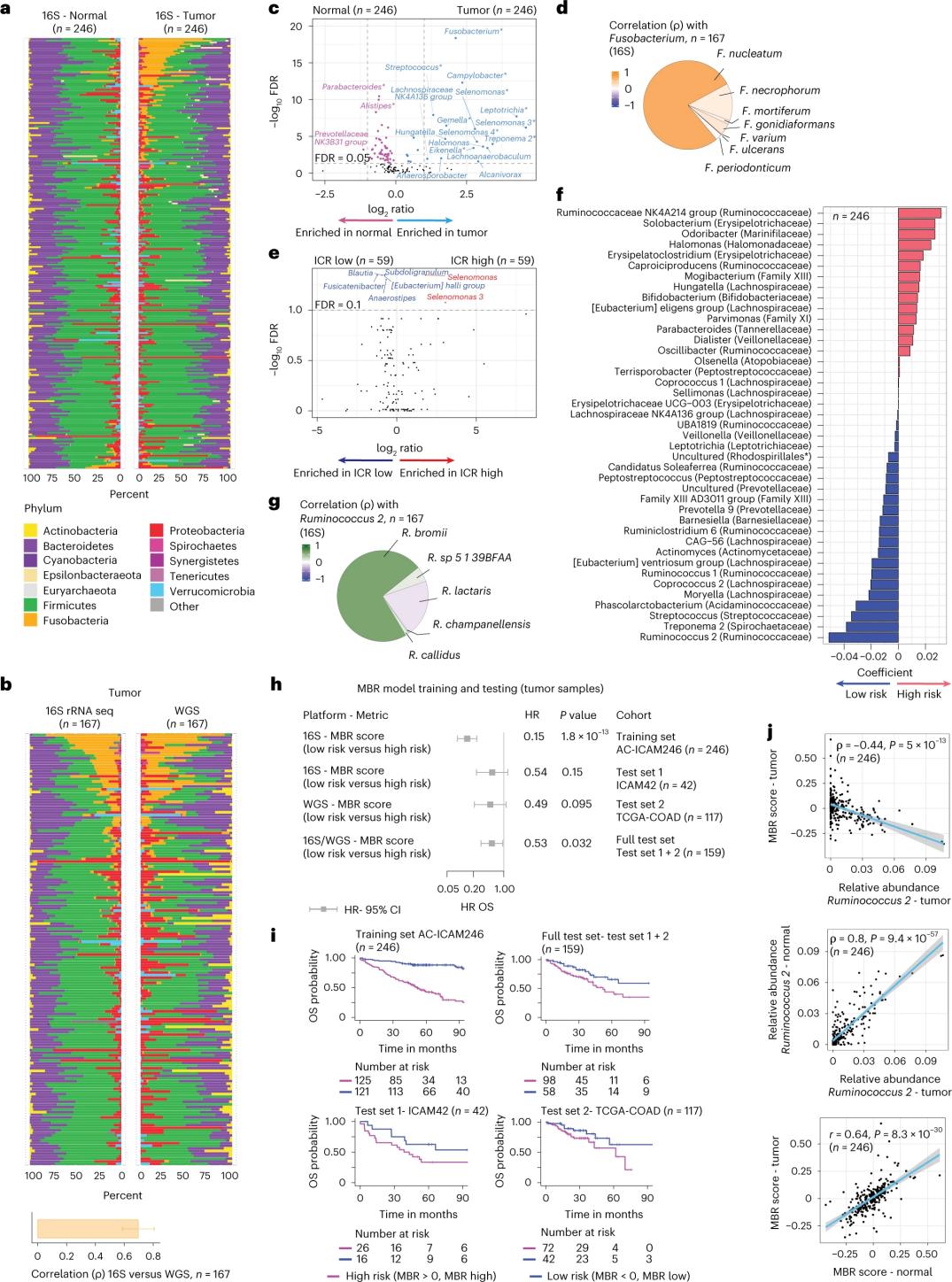
Figura 3. Microbioma en teixits tumorals i sans i la relació amb la ICR i la supervivència del pacient.
Conclusió
L'enfocament multiòmic utilitzat en aquest estudi permet la detecció i l'anàlisi exhaustives de la signatura molecular de la resposta immunitària en el càncer colorectal i revela la interacció entre el microbioma i el sistema immunitari. La seqüenciació profunda del TCR de teixits tumorals i sans va revelar que l'efecte pronòstic de l'ICR pot ser degut a la seva capacitat per capturar clons de cèl·lules T enriquides amb tumors i possiblement específiques d'antigen tumoral.
Mitjançant l'anàlisi de la composició del microbioma tumoral mitjançant la seqüenciació del gen 16S rRNA en mostres AC-ICAM, l'equip va identificar una signatura del microbioma (puntuació de risc MBR) amb un fort valor pronòstic. Tot i que aquesta signatura es va derivar de mostres tumorals, hi havia una forta correlació entre el colorectal sa i la puntuació de risc MBR del tumor, cosa que suggereix que aquesta signatura pot capturar la composició del microbioma intestinal dels pacients. Combinant les puntuacions ICR i MBR, va ser possible identificar i validar un biomarcador multiòmic d'estudiant que prediu la supervivència en pacients amb càncer de còlon. El conjunt de dades multiòmiques de l'estudi proporciona un recurs per comprendre millor la biologia del càncer de còlon i ajudar a descobrir enfocaments terapèutics personalitzats.
Data de publicació: 15 de juny de 2023
 中文网站
中文网站